Pool / Pool / Getty Images
Kľúčové jedlá
- FDA udelila povolenie na núdzové použitie vakcíne COVID-19 vyvinutej spoločnosťami Pfizer a BioNTech.
- Táto správa prichádza deň po tom, čo poradný výbor FDA odporučil agentúre povoliť vakcínu
- Podľa údajov preskúmaných výborom bola vakcína účinná na 95%.
- Distribúcia vakcín by mohla prísť do 24 hodín od autorizácie.
Úrad pre potraviny a liečivá (FDA) v piatok večer udelil povolenie na núdzové použitie svojej prvej vakcíne COVID-19. Vakcína vyvinutá spoločnosťou Pfizer Inc. a nemeckou spoločnosťou BioNTech sa začne distribuovať čoskoro.
Táto správa nasleduje po očakávanom verejnom vypočutí vo štvrtok, počas ktorého poradný panel FDA hlasoval 17: 4 za povolenie vakcíny Pfizer, jeden sa zdržal hlasovania.
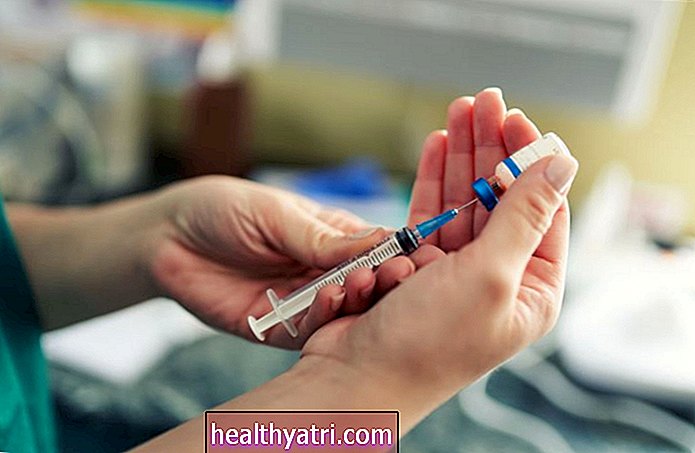
Spoločnosť Pfizer predstavila údaje z klinických štúdií, do ktorých bolo zapojených 43 000 dospelých účastníkov. Začiatkom tohto týždňa FDA zdieľala niektoré z týchto údajov, vrátane skutočnosti, že 95% ľudí v klinickom skúšaní, ktorí dostali vakcínu, nevyvinuli COVID -19. Vedľajšie účinky boli malé, vrátane zimnice, miernej bolesti a začervenania v mieste vpichu.
Povolenie na núdzové použitie (EUA) sa vzťahuje na osoby vo veku 16 rokov a staršie. Spoločnosť Pfizer taktiež vykonáva klinické skúšky bezpečnosti a účinnosti očkovacej látky u detí mladších ako 12 rokov a očakáva sa, že pridá aj skúšky pre mladšie deti.
Údaje o bezpečnosti a účinnosti z ďalších populácií, ktoré sú stále potrebné
Poradný panel FDA s názvom Poradný výbor pre vakcíny a súvisiace biologické výrobky (VRBPAC) odporúča spoločnosti Pfizer prijať ďalšie opatrenia na zaistenie bezpečnosti a účinnosti jej vakcíny pre viac populácií. Panel odporúča, aby sa do prebiehajúcich klinických štúdií pridalo viac ľudí farebných. U farebných ľudí bola vyššia pravdepodobnosť ako u Bielych ľudí, že sa nakazili vírusom COVID-19 a že zomreli na vírus.
Panel tiež diskutoval o dvoch hlásených prípadoch alergických reakcií u ľudí, ktorí dostali tento týždeň vakcínu vo Veľkej Británii, kde už bola schválená. MUDr. Paul Offit, riaditeľ Centra pre výučbu očkovacích látok v Detskej nemocnici vo Philadelphii, sa pýtal predstaviteľov spoločnosti Pfizer na alergické reakcie so znepokojením, že ľudia s ťažkými alergiami sa môžu rozhodnúť vakcínu nepodať. Spoločnosť Offit odporučila, aby sa uskutočnili štúdie o vakcíne aj u ľudí s bežnými alergiami.
Spojené kráľovstvo odporúča, aby ľudia, ktorí majú v anamnéze anafylaxiu liekov alebo potravín, vakcínu nedostali. USA môžu podobné varovanie pridať v tandeme s povolením. Pracovníci FDA na stretnutí informovali panel, že už pracujú na písomnej dokumentácii pre spotrebiteľov o bezpečnosti a účinnosti vakcíny.
Čo to pre vás znamená
Na základe odporúčania poradného výboru povoliť vakcínu Covid-19 od spoločnosti Pfizer mohol Úrad pre potraviny a liečivá schváliť jej použitie do niekoľkých dní. Distribúcia sa mohla začať veľmi skoro po tom.Očakáva sa, že prvé dávky vakcíny sa podajú zdravotníckym pracovníkom a obyvateľom ošetrovateľských domov.
Na základe rozhodnutia VRBPAC vydal komisár FDA Stephen M. Hahn, MD vyhlásenie:
„Za normálnych okolností proces preskúmania vakcín študovaných u desiatok tisíc ľudí trvá mesiace. Napriek tomu, že proces bol urýchlený v súvislosti s preskúmaním tejto EUA, odborníci FDA preskúmali tisíce stránok technických informácií [vrátane] údajov o klinických skúškach, neklinických údajov o vývoji vakcíny v laboratóriu, a výrobné údaje o tom, ako sa vakcína vyrába. “
Hahn, ktorý sa pravdepodobne snaží rozptýliť obavy spotrebiteľov, dodal: „V tejto veľmi naliehavej dobe pociťujú pracovníci FDA zodpovednosť za čo najrýchlejší postup procesu preskúmania. Vedia však, že musia vykonávať svoj mandát na ochranu verejného zdravia a na zabezpečenie toho, aby každá povolená vakcína spĺňala naše prísne normy bezpečnosti a účinnosti, aké Američania očakávajú. “
Novozvolený prezident Joe Biden po hlasovaní výboru vydal vyhlásenie, v ktorom uviedol: „K tomuto bodu nás viedla integrita vedy.“
FDA tvrdí, že distribúcia vakcín by mohla prísť do 24 hodín od autorizácie.
Poradný výbor FDA preskúma druhú vakcínu COVID-19 vyrobenú spoločnosťou Moderna vo štvrtok 17. decembra.