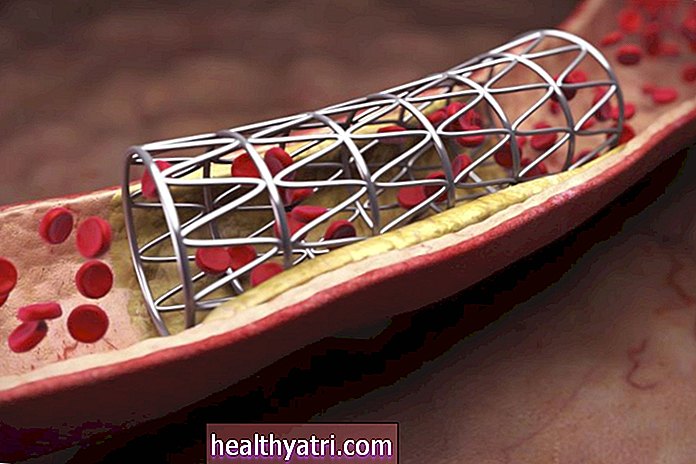
Na rozdiel od univerzálneho prístupu k liečbe rakoviny je presná medicína prístup, ktorý sa zameriava na konkrétne informácie o nádore človeka na účely diagnostiky a liečby choroby. Historicky sa liečba rakoviny líšila predovšetkým v závislosti od typu rakovinovej bunky pozorovanej pod mikroskopom.
Isaac Lane Koval / Corbis / VCG / Getty ImagesS ďalším porozumením ľudského genómu a imunológie bolo vyvinutých veľa nových terapií, ktoré sú zamerané na špecifické molekulárne zmeny a spôsoby rastu rakoviny alebo spôsoby, ako sa rakoviny naučili vyhnúť imunitnému systému. Génové profilovanie a sekvenovanie novej generácie môžu lekárom pomôcť nájsť podmnožiny ľudí s týmito typmi rakoviny, ktorí môžu reagovať na terapie, ktoré sa priamo zameriavajú na tieto zmeny.
V súčasnosti sa verí, že 40 až 50 percent druhov rakoviny je možné liečiť pomocou presnej medicíny.
Nasleduje podrobný popis fungovania presnej medicíny, požadované testovanie a niektoré príklady liekov, ktoré sa týmto spôsobom používajú na rakovinu.
Definícia
V minulosti sa rakovina delila primárne podľa bunkového typu, pričom v konkrétnom orgáne, napríklad v pľúcach, mohli vzniknúť možno dva alebo tri primárne typy rakoviny. Teraz vieme, že každá rakovina je jedinečná. Keby 200 ľudí v miestnosti malo rakovinu pľúc, malo by to z molekulárneho hľadiska 200 jedinečných druhov rakoviny. Na rozdiel od chemoterapie, liečby zameranej na elimináciu akýchkoľvek rýchlo sa deliacich buniek, presná medicína zahŕňa nové liečby zamerané na spôsob rastu rakoviny (cielené terapie) alebo spôsob, ako uniknúť imunitnému systému (lieky na imunoterapiu).
Národný rakovinový inštitút definuje presnú medicínu ako formu medicíny, ktorá využíva informácie o génoch, bielkovinách a prostredí človeka na prevenciu, diagnostiku a liečbu chorôb.
V prípade rakoviny precízna medicína využíva konkrétne informácie o nádore človeka, aby mu pomohla diagnostikovať, naplánovať liečbu, zistiť, ako liečba funguje, alebo urobiť prognózu. Príklady presnej medicíny zahŕňajú použitie cielených terapií na liečenie špecifických typov rakovinových buniek, ako sú napríklad HER2-pozitívne bunky rakoviny prsníka, alebo použitie testovania nádorových markerov na diagnostiku rakoviny.
Farmakogenomika je zase oblasť personalizovanej medicíny, ktorá sa zameriava na hľadanie liekov na liečbu špecifických genetických zmien v nádore.
Presnosť vs. prispôsobené
Pojmy presná medicína a trochu starší termín personalizovaná medicína sa niekedy používajú zameniteľné. Rozdiel je v tom, že starší termín znamenal, že liečba bola navrhnutá špeciálne pre každú osobu. Naproti tomu pri precíznej medicíne sa liečba zameriava na abnormality nádorov založené na genetických faktoroch, prostredí a životnom štýle.
Ako často sa dá použiť?
To, či sú k dispozícii možnosti presnej medicíny a koľko ľudí môžu ovplyvniť, sa môže pri rôznych druhoch rakoviny líšiť. Napríklad podľa Medzinárodnej asociácie pre štúdium rakoviny pľúc má asi 60 percent ľudí s rakovinou pľúc nádory s genetickými vlastnosťami, ktoré môžu mať k dispozícii liečbu precíznou medicínou. Ako je viac známe, je pravdepodobné, že sa tieto počty zvýšia.
Aj keď sa tu zameriavame na rakovinu, existujú aj ďalšie oblasti medicíny, v ktorých sa používa aj presná medicína. Jednoduchým príkladom je testovanie krvi človeka pred transfúziou krvi.
Diagnostické testy
Predtým, ako je možné liečiť nádor presnými liečebnými postupmi (farmakogenomika), je potrebné definovať molekulárne charakteristiky tohto nádoru. Na rozdiel od bežných testov, ako je napríklad sledovanie rakovinových buniek pod mikroskopom, musia sa nádory analyzovať na molekulárnej úrovni.
Molekulárne profilovanie vyhľadáva genetické zmeny v rakovinových bunkách, ako sú mutácie alebo zmeny usporiadania, ktoré pôsobia ako najväčšia slabosť rakoviny. Konkrétne tento druh profilovania hľadá mutácie alebo iné zmeny v génoch, ktoré kódujú proteíny, ktoré riadia rast nádoru alebo signalizujú dráhy nádoru.
Sekvenovanie novej generácie je zložitejšie ako molekulárne profilovanie. Hľadá širokú škálu genetických zmien, ktoré môžu súvisieť so širokou škálou druhov rakoviny.
Hovoriť o mutáciách v rakovinových bunkách môže byť veľmi mätúce, pretože sa hovorí o dvoch rôznych druhoch mutácií:
- Získané mutácie. Toto sú mutácie, ktoré sa detegujú pomocou molekulárneho profilovania nádorov. Vznikajú po narodení v procese, keď sa z bunky stane rakovinová bunka. Mutácia je prítomná iba v rakovinových bunkách a nie vo všetkých bunkách tela a je „cieľom“ tu diskutovaných cielených terapií.
- Dedičné mutácie (mutácie zárodočnej línie). Sú prítomné od narodenia a v niektorých prípadoch môžu zvýšiť riziko vzniku rakoviny. Aj keď sa tieto mutácie najčastejšie testujú, aby sa zistilo, či má človek predispozíciu na rakovinu alebo či sa vyskytuje v jeho rodine, cielenými terapiami sa s nimi nezaobchádza.
To znamená, že sa dozvedáme, že niektoré dedičné mutácie môžu ovplyvniť správanie nádoru. Liečba nádoru na základe týchto informácií (vrátane testovania familiárnych mutácií) teda patrí do oblasti precíznej medicíny.
Molekulárne profilovanie a sekvenovanie novej generácie hľadajú genetické zmeny v nádorových bunkách, ktoré môžu reagovať na cielené terapie. Ďalšou významnou novou formou liečby je však imunoterapia, čo sú lieky, ktoré fungujú zjednodušene a posilňujú imunitný systém.
Napríklad pri rakovine pľúc existujú v súčasnosti štyri lieky na imunoterapiu, ktoré sú schválené pre pokročilé ochorenie. Vieme však, že to nefunguje pre každého.
Niektorí ľudia majú veľmi dramatickú odpoveď na imunoterapeutické lieky, zatiaľ čo iní podľa všetkého nereagujú alebo sa ich rakovina ešte zhoršuje.
Aj keď je veda mladá, vedci hľadajú spôsoby, ako určiť, kto bude na tieto lieky reagovať, čo sa pod mikroskopom nedá určiť. V súčasnosti existujú dva prístupy k testovaniu citlivosti pacienta na imunoterapiu, je však nevyhnutne potrebný ďalší výskum:
- Testovanie PD-L1 môže niekedy predpovedať, kto bude reagovať na imunoterapiu, ale nie je to vždy presné. Aj ľudia s nízkou hladinou PD-L1 (proteín, ktorý potláča imunitný systém) niekedy reagujú veľmi dobre.
- Tumor Mutation Burden (TMB) sa nedávno vyhodnotil ako ďalšia metóda na predpovedanie odpovede. TMB je mierou počtu mutácií prítomných v nádore a tí, ktorí majú vyššiu TMB, často lepšie reagujú na imunoterapeutické lieky. To dáva zmysel, pretože imunitný systém je navrhnutý tak, aby napádal cudzí materiál (vrátane rakovinových buniek), a bunky, ktoré majú viac mutácií, sa môžu javiť ako abnormálnejšie.
Výhody
Najzrejmejšou výhodou presnej medicíny je, že umožňuje lekárovi prispôsobiť liečbu rakoviny na základe ďalších informácií o rakovinových bunkách.
To zvyšuje pravdepodobnosť, že osoba bude reagovať na liečbu, a zníži pravdepodobnosť, že bude musieť vyrovnať sa s vedľajšími účinkami liečby, ktorá nefunguje.
Jedným príkladom, ktorý to popisuje, je použitie eGFR inhibítora nazývaného Tarceva (erlotinib). Keď bola táto terapia prvýkrát schválená pre rakovinu pľúc, často sa predpisovala s mentalitou „všetko pre každého“, čo znamená, že bola predpísaná v mnohých rôznych prípadoch. Pri takomto použití odpovedal iba malý počet ľudí (okolo 15 percent).
Neskôr génové profilovanie umožnilo lekárom určiť, ktorí ľudia majú nádory s mutáciou eGFR a ktorí nie. Keď sa Tarceva podávala ľuďom so špecifickou mutáciou, odpovedalo oveľa väčšie množstvo ľudí (zhruba 80 percent).
Od tej doby boli vyvinuté ďalšie testy a lieky, aby sa mohol na liečbu ľudí s konkrétnym typom mutácie eGFR (T790M), ktorý by nereagoval na Tarcevu, použiť iný liek (Tagrisso). Nedávno sa tiež ukázalo, že Tagrisso je účinnejším liekom ako Tarceva na nádory rakoviny pľúc s mutáciami eGFR. S novšími generáciami a špecifickejšími spôsobmi liečby viac pacientov pozitívne reaguje na individualizovanú liečbu.
Výzvy
S precíznou medicínou je možné uvažovať ešte v začiatkoch a je s ňou spojené množstvo výziev.
Oprávnenosť. Aj keď sa v nádorových bunkách dajú nájsť mutácie (a je pravdepodobné, že ich bude ešte oveľa viac), sú k dispozícii cielené lieky, ktoré sa zameriavajú iba na podmnožinu týchto zmien - buď schválené lieky, alebo lieky dostupné v klinických štúdiách. Navyše, aj keď sa tieto lieky používajú na riešenie konkrétnej mutácie, nie vždy fungujú.
Nie každý je testovaný. Veda sa mení tak rýchlo, že mnoho lekárov nevie o všetkých dostupných možnostiach testovania, ako je sekvenovanie novej generácie. Mnoho ľudí bez testovania nevie, že má na výber. To je jeden z dôvodov, prečo je také dôležité dozvedieť sa viac o svojej rakovine a byť svojim vlastným obhajcom.
Odpor. Pri mnohých cielených terapiách sa časom vyvinie rezistencia. Rakovinové bunky nachádzajú spôsob, ako rásť a deliť sa, aby skutočne obišli inhibíciu cieľovým liekom.
Kontrola neznamená liečenie. Väčšina cielených terapií dokáže kontrolovať nádor po určitý čas, kým sa nevyvinie rezistencia - nelieči rakovinu. Po ukončení liečby sa rakovina môže opakovať alebo postupovať. V niektorých prípadoch však výhody niektorých imunoterapeutických liekov môžu pretrvávať aj po ukončení liečby a v niektorých neobvyklých prípadoch môžu vyliečiť rakovinu (známa ako trvalá odpoveď).
Nedostatočná účasť na klinických skúškach. Terapie musia byť testované skôr, ako budú schválené pre všetkých, a je zapísaných príliš málo ľudí, ktorí sa kvalifikujú do klinického skúšania. Menšinové skupiny sú tiež v klinických skúškach výrazne nedostatočne zastúpené, takže výsledky nemusia nevyhnutne odrážať výkonnosť lieku v rôznorodej skupine ľudí.
Náklady. Niektoré zdravotné poistenia nepokrývajú všetky alebo časť testov génovej profilácie. Niektoré pokrývajú testovanie iba na niekoľko mutácií, a nie na komplexnejšiu kontrolu, ako je testovanie spoločnosťou Foundation Medicine (spoločnosť, ktorá vykonáva genomické testovanie). Tieto testy môžu byť neúmerne drahé pre tých, ktorí musia platiť z vlastného vrecka.
Ochrana osobných údajov. Aby sme sa mohli posunúť vpred s precíznou medicínou, sú potrebné údaje od veľkého počtu ľudí. To môže byť náročné, pretože viac ľudí sa bojí straty súkromia, ku ktorej môže dôjsť pri genetických testoch.
Načasovanie Niektorí ľudia, ktorí by mohli mať nárok na tieto liečby, sú v čase diagnostikovania veľmi chorí a nemusia mať čas, ktorý je potrebný na vykonanie testov, čakanie na výsledky a podanie liekov.
Použitie a príklady
Rakovinu prsníka možno definovať v kategóriách na základe typov buniek pozorovaných pod mikroskopom, ako je duktálny karcinóm, ktorý vzniká v bunkách lemujúcich prsné kanály, a lobulárny karcinóm, ktorý vzniká v bunkách lalokov prsníka.
S rakovinou prsníka sa tradične zaobchádzalo, akoby išlo o jeden typ ochorenia, chirurgickým zákrokom, chemoterapiou a / alebo ožarovaním. Presná medicína teraz zahŕňa testovanie molekulárnych charakteristík nádorov.
Napríklad niektoré druhy rakoviny prsníka sú pozitívne na estrogénové receptory, zatiaľ čo iné môžu byť pozitívne na HER2 / neu. Pri HER2 pozitívnych rakovinách prsníka majú nádorové bunky zvýšený počet (amplifikáciu) génov HER2. Tieto gény HER2 kódujú proteíny, ktoré pôsobia ako receptory na povrchu niektorých buniek rakoviny prsníka. Rastové faktory v tele sa potom viažu na tieto receptory a spôsobujú rast rakoviny. Terapeutické terapie zamerané na HER2, ako napríklad Herceptin a Perjeta, sú zamerané na tieto proteíny, takže rastové faktory sa nemôžu viazať a spôsobiť rast rakoviny.
Rakoviny pľúc môžu byť pod mikroskopom rozdelené podľa bunkového typu, ako sú nemalobunkové karcinómy pľúc a malobunkové karcinómy pľúc. Teraz existujú zmeny, ktoré možno zistiť pri profilovaní génov a ktoré je možné liečiť presnou medicínou, vrátane mutácií eGFR, prešmykov ALK, prešmykov ROS1, mutácií BRAF a ďalších.
S pozitívnym karcinómom pľúc EGFR je v súčasnosti schválených niekoľko liekov. Rezistencia sa u väčšiny ľudí vyvinie včas (v dôsledku získaných mutácií), ale prechod na iný liek v tejto kategórii (napríklad lieky druhej alebo tretej generácie) môže byť efektívny. Napríklad niektorí ľudia sa stanú rezistentnými na Tarcevu (erlotinib), keď sa vyvinie mutácia T790M, a potom môžu reagovať na liek Tagrisso (osimertinib).
Dúfame, že časom, pomocou cielených terapií, ako sú tieto, a prechodom na liek novej generácie, keď sa vyvinie rezistencia, budú lekári schopní liečiť niektoré druhy rakoviny ako chronické choroby, ktoré si vyžadujú liečbu, ale dajú sa kontrolovať.
Väčšina liekov, ktoré spadajú pod presnú medicínu, účinkuje primárne na jeden typ rakoviny, ale existujú niektoré, ktoré môžu účinkovať pri rakovine. Prvým liekom, ktorý sa týmto spôsobom osvedčil, bol imunoterapeutický liek Keytruda (pembrolizumab), ktorý účinkuje na niekoľko druhov rakoviny.
Liečba Vitrakvi (larotrektinib) bola schválená ako prvá cielená terapia pôsobiaca na rakovinu. Zameriava sa na špecifickú molekulárnu zmenu nazývanú fúzny gén neurotrofického receptora tyrozínkinázy (NRTK) a bol účinný v 17 rôznych typoch pokročilých druhov rakoviny v klinických štúdiách.
Vedľajšie účinky
Vedľajšie účinky liečby presnou medicínou sa líšia v závislosti od liečby, ale niekedy sú výrazne miernejšie ako chemoterapeutické lieky.
Ako bolo uvedené, chemoterapia napáda všetky rýchlo sa deliace bunky, vrátane vlasových folikulov, buniek v gastrointestinálnom trakte a buniek v kostnej dreni - čo má za následok známe vedľajšie účinky. Pretože cielené terapie fungujú tak, že sa zameriavajú na špecifické cesty rastu rakovinových buniek, a imunoterapeutické lieky zlepšujú schopnosť imunitného systému bojovať proti rakovine zjednodušene, majú preto často menej vedľajších účinkov. Príkladom je liek Tarceva, ktorý sa používa na eGFR pozitívny karcinóm pľúc. Zvyčajne je dobre znášaný, s výnimkou vyrážok podobných akné a hnačiek.
Vieme, že každá rakovina je jedinečná a precízny liek využíva riešenie týchto jedinečných vlastností. Väčšina výziev súvisí s novotou vedy, ale s ďalšími informáciami a výskumom, dúfajme, nahradí univerzálny prístup k mnohým typom rakoviny.
Ako môže genómové testovanie zlepšiť liečbu rakoviny

-lowers-risk-of-invasive-breast-cancer.jpg)

-breast-cancer.jpg)