Ektopický sa týka predmetu alebo ľudského tkaniva, ktoré sa formuje alebo nachádza tam, kam nepatrí. Ektopická tvorba kostí je ukladanie nového kostného materiálu (procesom nazývaným osifikácia) v oblastiach, kam tento materiál opäť nepatrí. Tento proces osifikácie vykonávajú bunky nazývané osteoblasty.
Cecilie_Arcurs / Getty ImagesSlovo ektopické pochádza od Grékov a znamená „preč z miesta“. Jeho antonymum, ktoré je „ortotopickou“ kosťou - tiež odvodené z gréčtiny - sa podľa Scotta a kol. Vzťahuje na kosť, ktorá sa formuje na správnom anatomickom mieste. al., vo svojom článku s názvom „Stručný prehľad modelov formovania ektopickej kosti“. Článok bol publikovaný v marci 2012 v časopise,Vývoj kmeňových buniek.
Ektopická tvorba kostí môže byť prítomná pri narodení, môže byť dôsledkom genetiky alebo môže vzniknúť ako komplikácia určitých zdravotných stavov, ako je paraplégia a / alebo traumatické poranenie (spomenieme len niektoré). Scott a kol. al. hovoria, že sa predpokladá, že tvorba ektopickej kosti je spôsobená lokálnym zápalom, po ktorom nasleduje zhromaždenie kostrových progenitorových buniek. Podľa webovej stránky Bostonskej detskej nemocnice je progenitorová bunka veľmi podobná kmeňovej bunke, až na to, že je obmedzenejšia, pokiaľ ide o typy buniek, ktoré sa môžu pri delení stať. Progenitorové bunky pochádzajú z kmeňových buniek, ale nie sú to dospelé kmeňové bunky.
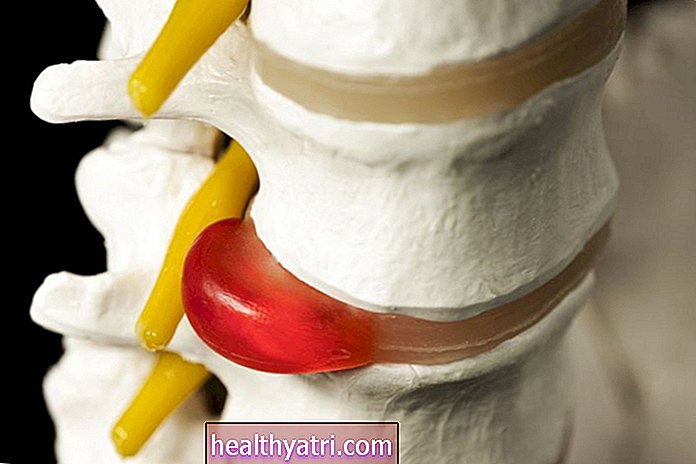
Ektopická tvorba kostí v dôsledku operácie chrbtice
Scott a kol. al, tvrdia, že až u 10% pacientov, ktorí podstúpia invazívny chirurgický zákrok - a operácia chrbta do tejto skupiny určite spadá - sa vyvinie ektopická tvorba kostí.
V chrbtici sa niekedy pojem „ektopická tvorba kostí“ používa na označenie nežiaduceho kostného tkaniva, ktoré sa ukladá v miechovom kanáli. V roku 2002 schválila FDA kostný proteín vyrobený spoločnosťou Medtronic s názvom Infuse na použitie pri operáciách bedrovej chrbtice. Kritériá použitia špecifikované FDA boli veľmi konkrétne: Ako kostný štep pre jednoúrovňovú prednú lumbálnu interbody fúziu (ALIF) v systéme systému Lumbar Tapered Fusion Device (LT-Cage).
Lenže krátko po schválení začalo veľa chirurgov používať materiál „mimo označenia“, čo znamená na iné účely, ako je schválené FDA. Nesprávne použitia zahŕňali operáciu krčnej chrbtice, ktorá viedla k hláseniu mnohých „nežiaducich udalostí“ alebo AE k FDA. Ektopická tvorba kostí bola jednou z AE, ale zoznam obsahoval ďalšie veľmi vážne veci, ako je arachnoiditída, zvýšený neurologický deficit, retrográdna ejakulácia, rakovina a ďalšie. Nepekné.
Kontroverzia Medtronic
TheMilwaukee Journal SentinalSpráva strážneho psa, ktorá sleduje tento príbeh od roku 2011 (a pokračuje v tom ďalej), tvrdí, že v priebehu niekoľkých týždňov od prvého klinického skúšania lieku Infuse sa zistila ektopická tvorba kostí u 70% pacientov v štúdii. Niektorí z týchto pacientov vyžadovali jeden alebo viac chirurgických zákrokov na odstránenie nežiaducej kosti a / alebo zdravotných komplikácií, ktoré z nej vznikli.
Vo svojom preskúmaní dôkazov uverejnených v čísle z roku 2013Surgery Neurology International, Epstein porovnal 13 priemyselných štúdií s inými štúdiami následne publikovanými v časopisoch, ako aj s dokumentmi a informáciami FDA nachádzajúcimi sa v databázach. Uvádza, že v štúdiách Infuse zistila „pôvodne nezverejnené nežiaduce udalosti a vnútorné nezrovnalosti“. Tiež uvádza, že 40% nežiaducich udalostí možno pripísať ALIF („off-label“ operácia krku, ktorá sa urobila), a dodáva, že niektoré z týchto udalostí boli život ohrozujúce.
MedzitýmMilwaukee Journal Sentineluvádza, že spoločnosť Medtronic v správe z roku 2004, ktorú napísali lekári financovaní spoločnosťou Medtronic, nedostatočne hlásila alebo vôbec nehlásila tieto nežiaduce účinky FDA. MJS tvrdí, že „lekári, ktorí napísali príspevok z roku 2004, budú naďalej dostávať autorské honoráre a ďalšie platby od spoločnosti Medtronic v hodnote miliónov dolárov.“
V máji 2014 MJS nadviazala na tento príbeh ďalším článkom, v ktorom uviedla, že spoločnosť Medtronic súhlasila so zaplatením 22 miliónov dolárov na vybavenie 1000 pohľadávok proti spoločnosti Infuse. V príbehu sa tiež spomínalo, že spoločnosť Medtronic vyčleňuje ďalších 140 miliónov dolárov na pokrytie „očakávaných škôd“.